ֵ���őе�ˮ̎���O(sh��)�乩��(y��ng)��
�����ṩ���I(y��)��ˮ̎�����g(sh��)����(w��)

������������(y��ng)�������ˮ����̎������100����Ěvʷ����Ŀǰ���ˮ�S���^��Ҋ���������g(sh��). Ȼ���ԏ�20���o(j��)70���Rook���Ȱl(f��)�F(xi��n)���ˮ���������и��a(ch��n)�����u����(THMs)���ɣ���NDBPs��m(x��)���z���������u���ᡢ �u���桢 �u��ȩ�� �u��ͪ�� �u����������ȣ�߀�ж�N���u��DBPs���灆�����. ���о������������(sh��)DBPs����(d��o)�����ˮ��“�°��� �»��� ��ͻ׃”���L(f��ng)�U���@���ӣ�߀�����T��(d��o)�²����a(ch��n)�������ؿ��Ի�������������B(t��i)��ȫ������{��ʹ���������İ�ȫ���ܵ��ˏV���P(gu��n)ע. ����������p���������^���Юa(ch��n)����DBPs���˂��Ⱥ��о��˳����� ���⾀�� �������ȵ�����������g(sh��)��Ȼ���@Щ�������g(sh��)�����ھ����ԣ�������� ��������������ˇ���Ծ���DBPs���ɵ��L(f��ng)�U�������������������߂�־õĚ���������. ��ˣ�̽�����ܱ������ˮ��ȫ������������Ҳ�ɞ��Щ����о����c.
�������^�����⛏�(f��)�Ϸ�(oxone��2KHSO5·KHSO4·K2SO4)��һ�N���͵��^�����������������еĻ��Գɷֺ��������܁�Դ����^������(KHSO5��Peroxymonosulfate��PMS)����(f��)�Ϸ���ͬ�r�o���Ȼ��c�ͱ�����Ԅ��ȳɷ�. ���^�����⛏�(f��)�Ϸ�����ˮ���ጷŰ���С�������ɻ��� �����B(t��i)���ڃ�(n��i)�Ķ�N������N���܉��Ɖ�����ļ���Ĥͨ������[22]; PMS�ɱ��������}�� �F�Ƚ����x�ӻ���a(ch��n)�����ɻ���ʹDNA ����������I���ѣ��ɔ_DNA��RNA�ĺϳ�[23]; ��������ԭ�w��ʹ�þ��w�����|(zh��)׃�����̣��Ķ����粡ԭ����. ���^�����⛏�(f��)�Ϸی������� ����� �����ȶ�N�²���������^���Ě�������[25]�����H����ʹ�õ�ˮ��Һ�����^�ͣ����ښW��������������. Ȼ��Ŀǰ�����^�����⛏�(f��)�Ϸ��������ˮ�����İ�ȫ�Ե��о����٣�Sánchez-Fortún �ȿ����˰������^�����⛏�(f��)�Ϸ��ڃ�(n��i)�ĎNˎ��������sˮϵ�y(t��ng)�������r���z�����ԣ��l(f��)�F(xi��n)���^�����⛏�(f��)�Ϸ���ԇ�l���µ��z�������^��.
�������Č����^�����⛏�(f��)�Ϸ��������^���е�DBPs�����L(f��ng)�U���z�������M���о����Ա������ɽ��ˮ�S�Mˮ�ͻ���̿�V�س�ˮ����ԇ���ˮ����ˮ�ӽ�(j��ng)���^�����⛏�(f��)�Ϸ����������ɵ�DBPs�M�ж��Է��������^�ˆ��^�����⛏�(f��)�Ϸۺ���������DBPs����������ͨ�^umuԇˮ����������z������׃���M�Мyԇ.
����1 �����c����
����1.1 ����
����ԇ�ˮ�Ӟ鱱�����ɽ��ˮ�S���Mˮ(ԭˮ)�ͻ���̿�V�س�ˮ(̿��ˮ). ˮ���ռ���2 h��(n��i)�\��������ң�����������0.45μm�VĤ�^�Vȥ���Ҹ���. ˮ����Ͷ��һ�������Ć��^�����⛏�(f��)�Ϸۺ��������]��ɫԇ��ƿ�У����Ҝؗl�����M����������(y��ng)������(y��ng)�r�g��24 h���Y(ji��)��������m����������c��Һ(2 500 mg·L-1)�Kֹ��������(y��ng). ��Ͷ�ӏ�(f��)�Ϸ�ǰ���ˮ���M�й�����ȡ����������HLB��(500 mg,6 mL,����OASIS)����5 mL�״���5 mL��ˮ�����3 mL���ȼ����3 mL��������������ϴҺ�M�и���. ϴÓҺ��(j��ng)������s���M��GC/MS���Է���.
������DBPs�������y����umu�yԇ�У�һ�Mԇ��Ԇ��^�����⛏�(f��)�Ϸ���������������һ�Mԇ�tͶ�Ӵ������c(������)���錦��. ��ˮ�ӷքeͶ��һ�������Ć��^�����⛏�(f��)�Ϸۺʹ������c�M����������(y��ng)������Һ������ȡ-����ɫ�V���y�����������u����(THMs)���u����(HAAs)��������.
����ͬ��ȡ���ɽˮ�Sԭˮ��̿��ˮ��ˮ���^�V��քeͶ�ӆ��^�����⛏�(f��)�Ϸۺʹ������c��������������c��Һ�Kֹ����(y��ng)�����}���{(di��o)��(ji��)ˮ��pH��2.0±0.1�����M�й�����ȡ. ��ȡ���ϴÓҺ�õ��ⴵ�ɣ��ö�������(DMSO)�ܽⶨ�ݣ��M��umu�z�����Ԝyԇ. umu�yԇ�x�������ɳ�T�Ͼ�TA1535/pSK1002���꣬���ձ��|��ˎ�ƴ�W(xu��)�ṩ. ��ԇ���4-�������-1-������(4-nitroquinoline-1-oxide��4-NQO)������Ԍ���.
����1.2 ���ԇ��
�������^�����⛏�(f��)�Ϸۣ��ɳɶ����d����ˎ�I(y��)����˾�ṩ; �������cˮ��Һ(��Ч�ȝ��≥5%�����W(xu��)��)�� ��������c(������)�� �}��(������)���ɇ�ˎ�ṩ; ԇ��������ЙC�܄��״��� ���嶡����(MtBE)�� �����顢 ��ͪ�� ���ȼ��顢 ���������Ⱦ���HPLC������J. T. Baker��˾�ṩ; DMSO(ACS��) ������Amresco��˾�ṩ;4-NQO(≥98%)�� ���u������u�����(bi��o)��(zh��n)���|(zh��)����Sigma-Aldrich��˾�ṩ.
����1.3 ��Ҫ�O(sh��)��
����ȫ�Ԅӹ�����ȡ�x��DIONEX AT280; Agilent 7890A����ɫ�V�x; Agilent 5975C�|(zh��)�V�x; ø��(bi��o)�x��MD SpectraMax M5; ������B(y��ng)�䡢 ø��(bi��o)����ʎ���B(y��ng)���� �x�ęC�� ˮԡ�����ʎ���� �����x��.
����2 �Y(ji��)���cӑՓ
����2.1 �������a(ch��n)�ﶨ�Է���
�����քe��ԭˮ��̿��ˮ��Ͷ��2.0 mg·L-1���^�����⛏�(f��)�Ϸۣ�����ǰ��ˮ�������ЙC�{(j��ng)GC/MS�����ĽY(ji��)��Ҋ�� 1�ͱ� 2��ʾ.
������ 1 ԭˮͶ�ӆ��^�����⛏�(f��)�Ϸ�ǰ��GC/MS�����Y(ji��)��
����
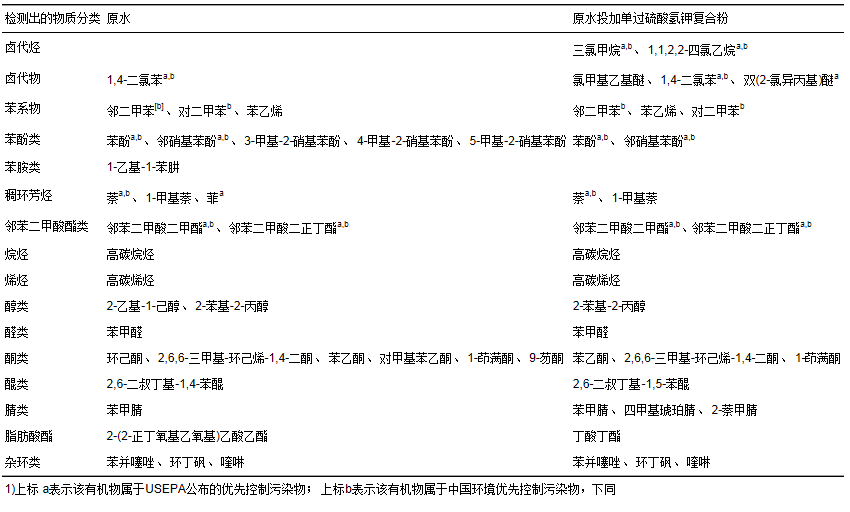
������ 2 ̿��ˮͶ�ӆ��^�����⛏�(f��)�Ϸ�ǰ��GC/MS�����Y(ji��)��
����

��������ԭˮ�д��ڵĸ�ֳ����y�]�l(f��)������ЙC�ﲻ��ͨ�^GC/MS�z����GC/MS�����H���ړ]�l(f��)�Ե�С�����ЙC��. ����(j��)��ԇ�Y(ji��)����ԭˮ�й��z�y��32�N�ЙC�������USEPA��(y��u)�ȿ�����Ⱦ�����ε���7�N�������҇���(y��u)�ȿ�����Ⱦ�����ε���8�N. �����е��ЙC��Ⱦ���У������廯����(������ϵ� ����� ����� ���h(hu��n)���N����������������)����18�N����ԭˮ����Ҫ����Ⱦ����ͣ���Ξ�ͪ�(4�N)�� �s�h(hu��n)�(3�N)���������������(2�N). ԭˮͶ�ӆ��^�����⛏�(f��)�Ϸۺ������ˎNԭˮ�Л]�е��u���N���u����������ȼ��顢 1,1,2,2-�������顢 �p(2-�Ȯ�����)�Ѻ��ȼ��һ��ѣ�ǰ���߾���USEPA�����ă�(y��u)�ȿ�����Ⱦ��.
�����ɱ� 2�Y(ji��)����֪��̿��ˮ�д��ڵ��ЙC��N�����ԭˮ�^�٣����z�y��25�N�ЙC�����7�N������USEPA��(y��u)�ȿ�����Ⱦ�����Σ�8�N�������҇���(y��u)�ȿ�����Ⱦ������. ̿��ˮ�����ЙC��Ⱦ���У������廯�����Ԟ���Ҫ��Ⱦ��ͣ����z��14�N. ̿��ˮ��Ͷ�ӆ��^�����⛏�(f��)�Ϸ�֮���˱������е�1,1,2,2-�������顢 1,4-���ȱ����p(2-�Ȯ�����)���⣬��������DBPs���ȼ�����������.
���������(sh��)DBPs���Н����°��� �»��� ��ͻ׃�ԣ������ˮ��ȫ������{. �����Ϸ����Y(ji��)�����Կ�����ˮ����Ͷ�ӆ��^�����⛏�(f��)�Ϸ�֮���ЙC��Ⱦ��ĽM��׃�����������µ��u���N���u�������ɣ�ʹ��������ˮ�w����һ���İ�ȫ�L(f��ng)�U.
����2.2 �������a(ch��n)���������y��
�������u����(THMs)���u����(HAAs)���Ȼ������^�̮a(ch��n)���ă����Ҫ��DBPs�����u�rDBPs�°��L(f��ng)�U����Ҫָ��(bi��o)����(sh��)[29]. ���^�����⛏�(f��)�Ϸ��к���NaCl���o���ɷ�. Lente��[30]�о�PMS�c�u�صķ���(y��ng)���l(f��)�F(xi��n)PMS���Ա��u�ػ�a(ch��n)��OX-(X��Cl�� Br �� I). ���ٵ�[31]��ԇ��C������(d��ng)ˮ��Cl-�ĝ���^�͕r��PMS����ֱ���cCl-�M�з����ɻ�����(y��ng)���ɻ�����NCl2��HOCl����ʽ(1)�c(2)��ʾ. ��ˮ�(d��ng)���^�����⛏�(f��)�Ϸ�����ˮ�r�����ڏ�(f��)�Ϸ���NaCl�Ĵ��ڣ�ʹ�Ï�(f��)�Ϸۿ���ጷ�һ�����Ĵ����ᣬ�Ķ����������u��DBPs�Ŀ���.
����
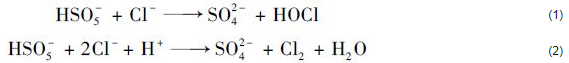
������ԭˮ��̿��ˮ�зքeͶ�ӆ��^�����⛏�(f��)�Ϸ۴������c����(f��)�Ϸ�Ͷ������2.0 mg·L-1���������cͶ�Ӻ�����ʼ��Ч�ȝ��Ҳ��2.0 mg·L-1. ˮ�ӽ�(j��ng)��������(y��ng)���THMs��HAAs�������y���Y(ji��)��Ҋ�D 1�͈D 2.
����

����
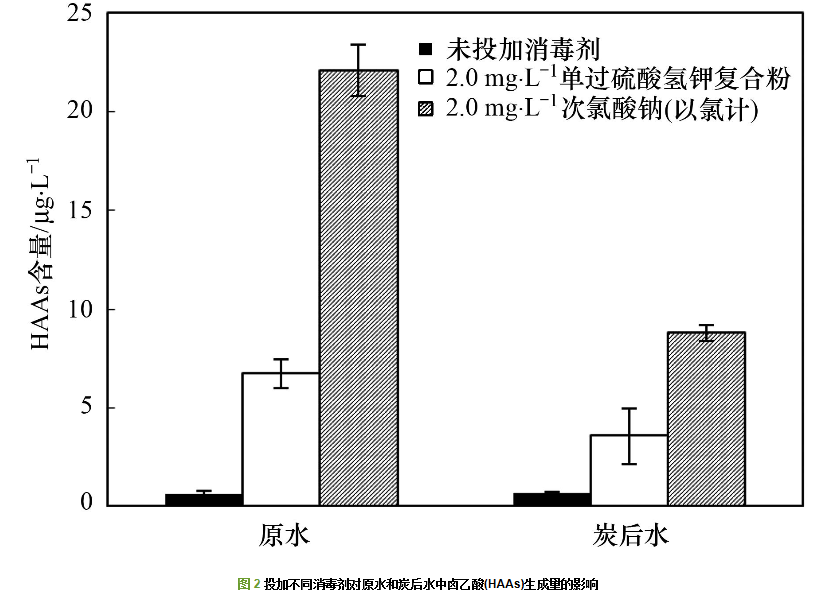
�����ɈD 1�͈D 2���Կ�����ԭˮ��̿��ˮͶ�ӃɷN��������ˮ���ЙC���c�ɷN���������l(f��)������(y��ng)������DBPs������THMs��HAAs��������ԭˮ��̿��ˮ�����@����. ԭˮ��THMs��HAAs�����քe��1.41 μg·L-1��0.59 μg·L-1��Ͷ��2.0 mg·L-1���^�����⛏�(f��)�Ϸۺ�THMs��HAAs���������8.98 μg·L-1��6.72 μg·L-1������(y��ng)��Ͷ�Ӵ������c����ߺ�������18.54 μg·L-1��22.06 μg·L-1. ����̿��ˮ���ԣ�Ҳȡ�������Ƶ�ԇ�Y(ji��)��.
�����ı�ԇ�Y(ji��)�����Կ������mȻ���^�����⛏�(f��)�Ϸ������^��Ҳ�ɮa(ch��n)���u������DBPs����Ͷ�Ӵ������c��ˮ�е�THMs��HAAs��������Ͷ�ӆ��^�����⛏�(f��)�Ϸۺ����������2~4����Ͷ�ӆ��^�����⛏�(f��)�Ϸ���������������a(ch��n)����DBPs����.
����2.3 �z�������u��
���������(sh��)�P(gu��n)��DBPs�L(f��ng)�U���о����ǻ��ڌ�����M�еĶ���W(xu��)�о����Д��. Ŀǰ�z������W(xu��)����ԇ�Ĝyԇ������Ҫ��Amesԇ ��ԇ ����ԇ��umuԇ��. ���о�����umuԇ�ķ��������^�����⛏�(f��)�Ϸ������^�̵�DBPs���z�������M�з���. ԇ�yԇ�Y(ji��)�����T��(d��o)��Irֵ��ʾ����������|(zh��)4-NQO�ĵȮ�(d��ng)�����ԁ��u�r���ˮ���°��L(f��ng)�U.
��������4-NQO��С����°�����Ч��(y��ng)��������õ����˵Ą���Ч��(y��ng)�������õ����˵��°�����ϵ��(sh��)(q=0.369 kg·d-1·mg-1). ���O(sh��)��Ʒ����Ⱦ����°�Ч��(y��ng)�c4-NQO��ͬ�����^ԇ�����Ԍ��պ͘�Ʒ�Ą���Ч��(y��ng)�P(gu��n)ϵ������б�ʣ��õ���Ʒ��4-NQO�Ȯ�(d��ng)�����TEQ(ng·L-1)���Ķ��_����Ʒ���°��L(f��ng)�U��С. ���������w��70kg��ÿ���ˮ2LӋ�㣬����umuЧ��(y��ng)�°��L(f��ng)�U��:
����
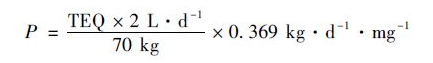
����ʽ��,P���°��L(f��ng)�U. ��(d��ng)�z������Ч��(y��ng)���°��L(f��ng)�U����f��֮һ(��P=10-6)�r��ˮ�е��z�����Ԯ�(d��ng)�����TEQ(��4-NQOӋ����ͬ)��94.8 ng·L-1�����о��Դ˞鰲ȫ�L(f��ng)�U�ֵ���yԇ�Y(ji��)���M���u��.
������2 L�^�V���ԭˮ�� 5 L�^�V���̿��ˮ�зքeͶ�ӄ�����0.1�� 0.5�� 1.0�� 2.0 mg·L-1�Ć��^�����⛏�(f��)�Ϸۺ���ʼ��Ч�ȝ�Ȟ�0.1�� 0.5�� 1.0�� 2.0 mg·L-1�Ĵ������c������������Ͷ�������z�����Ե�Ӱ푣��yԇ�Y(ji��)�����D 3�͈D 4��ʾ.
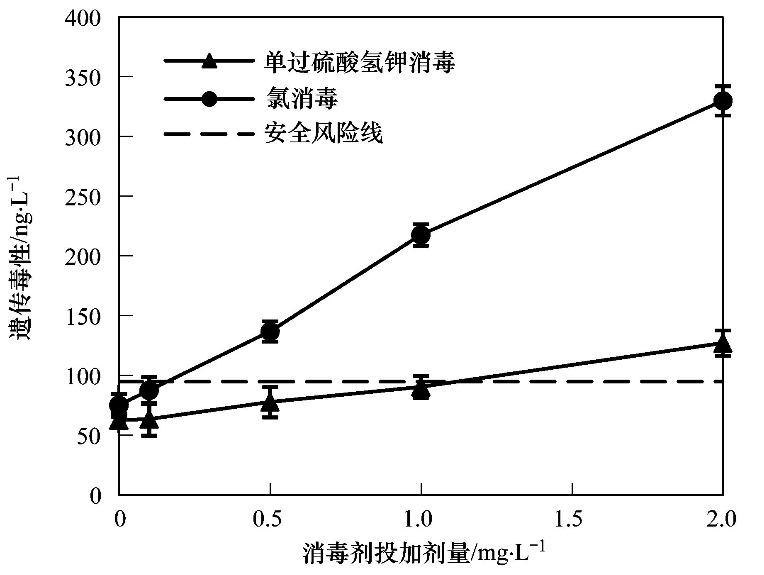
�����D 3 Ͷ���Ⱥ͆��^�����������ۺ�ԭˮ �z�������S������Ͷ������׃��
����
�����D 4 Ͷ���Ⱥ͆��^�����������ۺ�̿��ˮ�z�������S������Ͷ������׃��
����
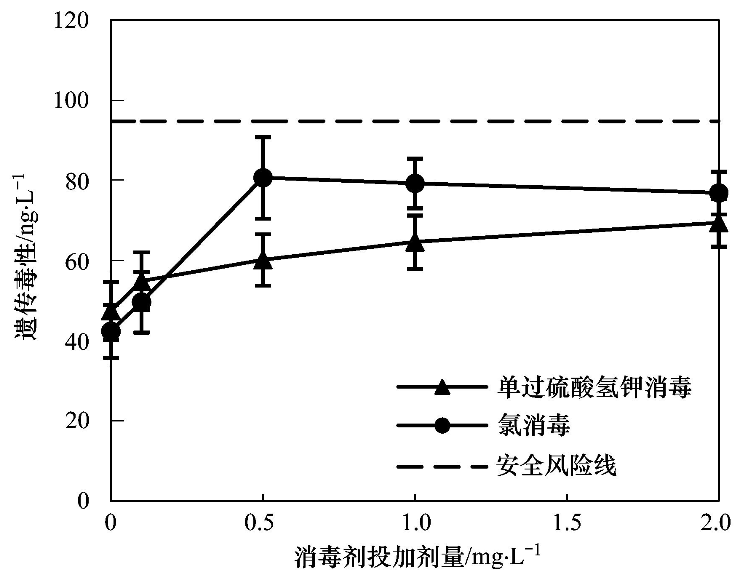
��������(j��)�yԇ�Y(ji��)����ԭˮ��̿��ˮ����������һ�����z������. Ͷ�����������S�����������������ӣ�����̿��ˮͶ�����������z�������������S�������½�������ԭˮ��̿��ˮ���z�����Ծ��S֮����. ����ԭˮ���ЙC�ﺬ���ͷN��^�࣬�������c���������ã�ʹ��ԭˮ���z�����ԏ���̿���ˮ.
����ԭˮ���ȵ�Ͷ�����_��0.5 mg·L-1�r���z�����Ԯ�(d��ng)����Ȟ�137.0 ng·L-1���Ѹ��ڰ�ȫ�L(f��ng)�U�ֵ(94.8 ng·L-1)���S����Ͷ�����������z�����Գ��^��������L��څ��. ԭˮ��Ͷ������������z���������@���چ��^�����⛏�(f��)�Ϸ��������������@���ڰ�ȫ�L(f��ng)�U�ֵ. ���چ��^�����⛏�(f��)�Ϸ�Ͷ�����_��2.0 mg·L-1�r���z�����Ԯ�(d��ng)����Ȟ�127.1 ng·L-1�����^�˰�ȫ�ֵ���f����(d��ng)ˮ���ЙC���^���r����߆��^�����⛏�(f��)�Ϸ۵�Ͷ����Ҳ������һ����ȫ�L(f��ng)�U.
������ԇ�Y(ji��)��������̿��ˮ���������͆��^������(f��)�Ϸ���������z�����Ծ����ڰ�ȫ�L(f��ng)�U�ֵ���������������z�����Ը��چ��^�����⛏�(f��)�Ϸ�������
����3 �Y(ji��)Փ
����(1) ͨ�^GC/MS���Է������yԇˮ����Ͷ�ӆ��^�����⛏�(f��)�Ϸ�֮���mȻ�ЙC��Ⱦ��ĽM��׃�����������µ��u���N���u�������ɣ�ʹ��������ˮ�w����һ���İ�ȫ�L(f��ng)�U.
����(2) �yԇˮ�ӽ�(j��ng)������������u����(THMs)���u����(HAAs)���������@���ڽ�(j��ng)���^�����⛏�(f��)�Ϸ��������������. ���^�����⛏�(f��)�Ϸ��������mȻ��DBPs���ɣ����京���^�ͣ������@����������.
����(3) ͨ�^umu���Ԝyԇ��ˮ�ӽ�(j��ng)����������z�����Ը��ڽ�(j��ng)���^�����⛏�(f��)�Ϸ��������z������. ����ˮ�����ЙC�ﺬ���^���r������������z�������S������Ͷ������������������@�������^�����⛏�(f��)�Ϸ���������z�����Ԅt��������. Ȼ����(d��ng)ˮ���ЙC���^���r���^��Ć��^�����⛏�(f��)�Ϸ۵�Ͷ����(���О�2.0 mg·L-1)Ҳ������һ���İ�ȫ�L(f��ng)�U.
����

������ˮ̎���O(sh��)��(li��n)ϵ��ʽ��
�����N�۟ᾀ��010-8022-5898
�����֙C̖�a��186-1009-4262
������ˮ̎���Ŀ�W(w��ng)ַ��http://bw5f.com/ws/