����������ҽ�B����——Ⱦ�ϏUˮÓɫ����
����һ������(Introduction)
�����S�������Ŀ��ٰlչ���҇��ѳɞ�Ⱦ�����a��������S֮�����a���˴�����Ⱦ�ϏUˮ.���˴���������Ⱦ���⣬Ⱦ�ϏUˮ��߀���������ж��к��ɷ֣����ؽ����x��.��ˣ�Ⱦ�ϏUˮ���гɷ֏��s��ɫ�ȡ���ȸߡ��y���オ�⡢ˮ��ˮ�|׃��������c���ɞ��^�y̎���Ĺ��I�Uˮ֮һ��
������ȸ�G�dz�Ҋ�������������Ⱦ��֮һ��������z��Ʒ��ë��Ʒ�����ȵ�Ⱦɫ��.�mȻ��ȸ�G���и߶��ԡ���ͻ׃�Ժ��^�������ﶾ�Ե����ԣ�������ɱ�����������Ч���@������ˣ�Ŀǰ�Ա��V�������ڼ�����ˮ�a�Bֳ�I.�ؽ���ͨ�������ڼ���Ⱦ�Ϲ��I�IJ�ͬ���a�^���У���ˣ�Ⱦ�ϏUˮ�д��ڸ��N��ͬ��ȵ��ؽ��٣����У�Cr(��)�ĺ������^�ߣ���Cu(��)��֮.�о��l�F���O�������ؽ����x�Ӿ��ܮa�����@���ж���������ͨ�^ʳ��朱��^��������ɱ��ظ������w�ȣ��ҕ�ʹ�����w�ȵ�ø�������|��ʧ�ͬ�r���o�������オ�⣬���^�K�۷e�������У����ؓp�������w���������B�h����Ⱦ�ϏUˮ�К���Ⱦ���c�ؽ����x�ӽ������棬�@�N�ͺ���Ⱦ���и��ߵ�����������ԡ�
����Ⱦ��Óɫһ��֞��������W����������ﻯ��ʹ�÷��㡢ҊЧ�죬���ɱ��ߡ�������Ⱦ����;����\���M�õͣ�̎��Ч���@���Ҳ�����ɶ�����Ⱦ���ǭh���Ѻõ�̎������������ܵ��V���Pע�����ؽ���ͨ�^Ӱ������w��ø�����ɻ�ø�Ļ����������Ⱦ�ϵĽ��⡣��ˣ�������Ⱦ���c�ؽ��٘��ɵďͺ���Ⱦ��Ⱦ�ϵ����オ��Ч�ʳɞ�ԓUˮ̎�����y�c֮һ.
����EDTA(�Ҷ�����������c)��һ�N��Ҋ�����τ������ɵĽj���������Ի�A�ԗl���·���ϵ���dz���.��һ����r�£��@Щ���������ϱȶ���1:1(�Ϸ��, 2011).EDTA�c��λ�x���γɭh��Y���������x��ȡ����λԭ���ϵĚ���M�����ϭh�У�ʹ�����x���g���������䶾�����á���Ŀǰ�P�ڲ��íh���ЏV�����ڵ����τ��p���cȾ�Ϲ�����ؽ����x�ӵĶ��ԣ����Ⱦ�Ͻ���Ч�ʵ��о����Ј��.����֮ǰ���о��l�F��ijЩ������ܕ���Cr(��)߀ԭ��Cr(��)����ˣ����о��M����EDTA����Cr(��)�Ķ��ԣ��Ķ����Cr(��)����r���オ���ȸ�G��Ч��.���úY�x���ĸ�Ч������Burkholderia cepacia C09G�����ȸ�G���о�EDTA���ؽ��ٹ���r�����ȸ�G��Ӱ푣�ͬ�r����EDTA����Cr(��)�ı��^�ѝ��.ͨ�^���о���������ؽ��ٹ���rȾ�ϵ�ȥ��Ч�ʣ�����s�Uˮ�������춨һ������Փ���A.
�������������c����(Materials and methods)
����2.1 ԇ���c�x��
����ԇ���������ǡ�KH2PO4��Na2HPO4·2H2O��MgSO4��FeCl3·6H2O��KNO3����ȸ�G(MG)��K2CrO7��EDTA�Ⱦ��������.
�����x����SKY-2102����ʽ�p�Ӻ�����B�u����SPX-2508-Z���������B�䡢722N�Ϳ�Ҋ����Ӌ��PHS-3C�;���pHӋ��AA-240��ԭ�����չ��V�x.
����2.2 ԇ���N�c���B��
������ԇ����þ��N��Burkholderia cepacia C09G(B. Cepacia C09G).LB���B����ţ���5 g·L-1��������10 g·L-1��NaCl 10 g·L-1�����b��100 mL�����ǟ�ƿ�У�ÿƿ�b����30.0 mL��121 ����15 min.�������B����������6.0 g·L-1��KH2PO4 1.8 g·L-1��Na2HPO4·12H2O 3.5 g·L-1��FeCl3·6H2O 0.01 g·L-1��MgSO4 0.1 g·L-1��KNO3 3.5 g·L-1���{����pH 6.0�����b��250 mL�����ǟ�ƿ�У�121 ����15 min.
����2.3 ԇ��2.3.1 ��Һ���Ƃ�
����������B. Cepacia C09G�ӷN��������LB���B���У���30 �桢150 r·min-1�ĺ����ʎ���B�������B�������ڣ��������þ�Һ�D����50.0 mL�x�Ĺ��У�7000 r·min-1�x��10 min����������Һ���ßo��ˮϡጳɾ���Һ��4 �汣�����.
����2.3.2 MG��Cr(��)ȥ��ԇ�
������������w�e��ˎƷ���뽵�����B���У�ÿ֧�����x�Ĺ�(�o��)�м���15.0 mL�Ľ������BҺ���ټ����Һ(��ʼOD600=0.7���w�e��6%)����������������u��(150 r·min-1��30 ��)���B0��12��24��36��48��60 h��քe�y��OD600��MG��Cr(��)���.����ÿ��ԇ����3��ƽ�У��Y��ȡ��ƽ��ֵ����Ӌ��˜�ƫ��.
����2.4 ��������MG��Cr(��)�Ĝy��
�����ĺ�ؓu����ȡ�����r�εĽ������B�����ڱ��^�����ղ��L600 nm̎�ÿ�Ҋ�ֹ���Ӌ�y������ȣ��Բ��L600 nm̎�Ĺ��ܶ�OD600��ʾ�������L��.
����ȡ����Һ����ȸ�G(MG)���÷ֹ���Ӌ�y��619 nm̎���^�����շ�������ֵ����A619��ʾ;����ԭ�����չ��V�x�y����Һʣ��Cr(��)���.ȥ����RӋ�㹫ʽ���£�
����
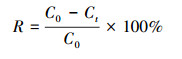
����(1)
����ʽ�У�C0��ʾ��ʼ�rMG��Cr(��)�ĝ��(mg·L-1);Ct��ʾt�rMG��Cr(��)�ĝ��(mg·L-1).
����2.5 ����
������������@�R(SEM)�^�죺����JSM-7500�͒�������@�R�^���Ʒ�ı�����ò���^�ΑB;X�侀����ɫɢ�V(EDS)�����������cSEM�C��X�侀����ɢ��x������Ʒ�����Ԫ�طNͺ���;�����~׃�Q�t����V(FTIR)����������Thermo Nicolet 5700�t����V�x���@ȡԇ�ӵ�FTIR�V�D���廯⛉�Ƭ�����跶����4000~400 cm-1;X�侀��������V(XPS)����������VG ESCALAB 250��X�侀��������V�x��������ȸ�G��Cr(��)���Burkholderia cepacia C09G�M�з���.
���������Y���cӑՓ(Results and discussion)
����3.1 ��ͬ�l������ȸ�G�����^�̵�Ӱ�
�������Ќ�����Burkholderia cepacia C09G����0.1 mmol·L-1��ȸ�G���H�����ȸ�G�Ğ�հ���������ٷքe����0.5 mmol·L-1 Cr(��)��0.5 mmol·L-1 EDTA���Լ�ͬ�r����0.5 mmol·L-1 Cr(��)��0.5 mmol·L-1 EDTA������u���к������B0��12��24��36��48��60 h��ȡ���y��OD600��A619��Cr���.
����3.1.1 OD600
������D 1��ʾ���ڿհ����(�]���ؽ���Cr(��)����EDTA���ڵėl����)�����H����0.1 mmol·L-1�Ŀ�ȸ�G(MG)�r��B. Cepacia C09G��ǰ36 h�������L��OD600�ӽ���0.7���������MG���������꣬ȱ���I�B���|���������L������60 h����^�KOD600ֵ��0.78;�H����0.5 mmol·L-1 Cr(��)������������L�к����������ã��������ܵͣ��H��0.15;�H����0.5 mmol·L-1 EDTA�������mȻ��Cr(��)��С��������һ�����������ã�60 h�rOD600��0.31.�������EDTA��EDTA-Metal���������ﶼ���ж���(Grcman et al., 2001).��ͬ�r����EDTA��Cr(��)�r��OD600��0.42�����چΪ�����Cr(��)����EDTA�r���f�������ﶾ�ԱȆΪ�����Cr(��)��EDTA�������ͣ���ˣ������ƜyEDTA������Ч����Cr(��)�Ķ���.
����
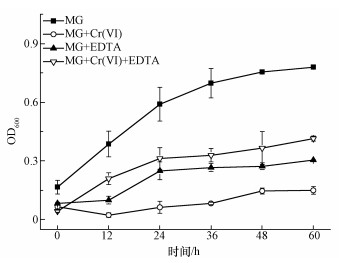
�����D 1��ͬ�l���¿�ȸ�G(MG)��OD600ֵ
����3.1.2 ��ȸ�G(MG)ȥ����
�����D 2a�鲻ͬ�l������ȸ�G�Ľ���Ӱ푣��ڃH����0.1 mmol·L-1 MG����r�£�MG��24 h��ȥ�����_��96.2%;ֻ����0.5 mmol·L-1 Cr(��)��60 h�rMG��ȥ���ʾ���6.7%���Ϊ�����0.5 mmol·L-1 EDTA�r��60 h�rMG��ȥ���ʞ�48.4%���f��Cr(��)��EDTA��������B. Cepacia C09G����ȸ�G�Ľ���.ͬ�r����EDTA��Cr(��)�r��60 h MG��ȥ����������18.8%�������چΪ���Cr(��)�Ľ�����������ߣ����Կ�����EDTA�_��������Ч�ؽ���Cr(��)���������ã��Ķ���ߌ���ȸ�G�Ľ���Ч��.Ҳ���о��C��������EDTA���Խ���5 μmol·L-1 Cd��Cu��Zn������Escherichia coli�Ķ���(Campbell et al., 2000).
����
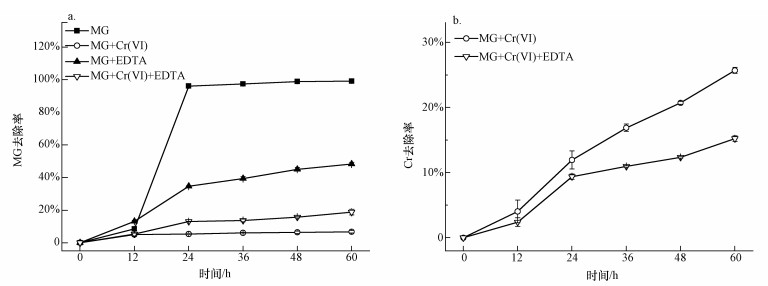
�����D 2��ͬ�l���¿�ȸ�G������(a)��Crȥ����(b)
����3.1.3 Crȥ����
�����D 2b���x�ĺ�Ľ������B���п�Cr��ȣ�����������EDTA������Ч����Cr����ˣ��p����B. Cepacia C09G����Cr��Ч�ʣ�ȥ���ʏ�25.7%���͵�15.2%.
����3.2 0.5 mmol·L-1 EDTA���ϵı��^��Cr���
����������C09G�����ʼCr(��)��ȷքe��0.5��0.6��0.7��0.8��0.9 mmol·L-1��EDTA��Ȟ�0.5 mmol·L-1��MG��Ȟ�0.1 mmol·L-1�Ľ������B���У�����u���к������B0��12��24��36��48��60 h��ȡ���y��OD600��A619��Cr�ĝ��.
����3.2.1 OD600
������D 3a��ʾ���S������Cr(��)��ȵ����ߣ�������OD600�����ߺͣ�����Cr(��)��Ȟ�0.7 mmol·L-1�r�_�����^��.�ڼ����Cr(��)��ȷքe��0.5��0.6��0.7��0.8��0.9 mmol·L-1�r��60 h�rOD600�քe��0.45��0.55��0.72��0.62��0.43���������L���ã���ˣ�EDTA���m�ȵؽ���Cr�Ķ���.�����ā��f��Cr�Ϊ����ڣ������cEDTA�γ�����������ﶼ���ж��ģ������������ƫ��.
����
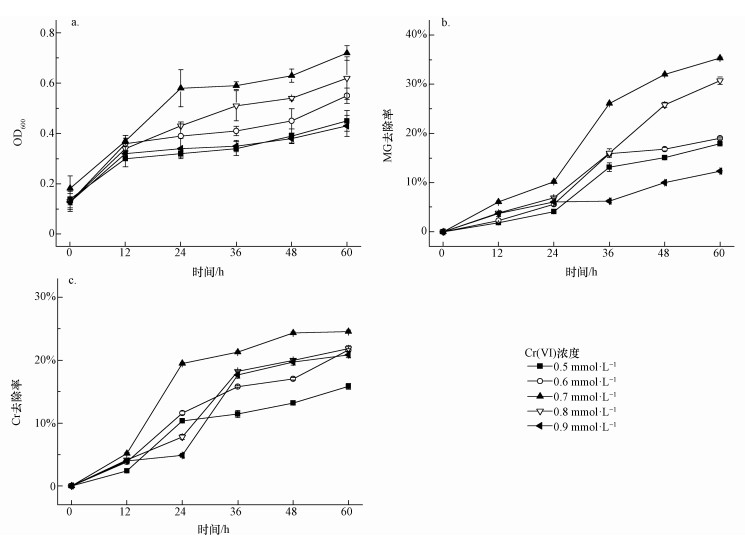
�����D 3��ͬ��ʼCr(��)�����OD600ֵ(a)����ȸ�G������(b)��Crȥ����(c)
����3.2.2 ��ȸ�G(MG)ȥ����
�����ɈD 3b��֪����Cr(��)��Ȟ�0.7��0.8 mmol·L-1�⣬����Cr(��)��ȗl���µ�MG���Ⲣ�����룬��С��20%;��Cr(��)��ʼ��Ȟ�0.7 mmol·L-1�r��MG��ȥ���ʞ�35.3%����������ӵ�0.8 mmol·L-1�r��MG�Ľ������½�����30.7%.��ˣ��_��0.5 mmol·L-1 EDTA�����£����ϵı��^��Cr(��)��Ȟ�0.7 mmol·L-1. EDTA���ؽ��ٵ����ϱ���һ���1:1(�Ϸ��, 2011)��Cr(��)����x�Ӵ��ڣ����ܺ�EDTA���ϣ������������Cr(��)��������߀ԭ��Cr(��)(�����, 2014).����Ɯy������Cr(��)��������߀ԭ��Cr(��)����߀ԭ��Cr(��)��EDTA���ϣ��p���˶���.EDTA����Cr(��)�^����MGȥ���ʶ�������.
����3.2.3 Crȥ����
������D 3c��ʾ��Cr(��)��ʼ��ȷքe��0.5��0.6��0.7��0.8��0.9 mmol·L-1�r����Cr��ȥ���ʷքe��15.8%��21.6%��24.6%��21.8%��20.9%.Crȥ�����S�������Cr(��)������Ӷ����ӣ���Cr(��)��0.7 mmol·L-1�rCrȥ���ʱ��^�ߣ�֮���_ʼ�½��������ͷ��Ⱥ�С.���������ߝ�ȵ�Cr���|Ч�����ã���������ڱ����︻��.�����ڟoEDTA������r�£�B. Cepacia C09G��Cr�����������½������ڱ��^�ѵ����ϝ���£����ڜp����Cr�Ķ��ԣ���������������ʹ���������������.�����ā��f����EDTA���ڗl���£�B. Cepacia C09G��Cr�����������^��.
����3.3 �����^�̵ı���3.3.1 XPS
�������˙z�yCr(��)�r�B׃��������X�侀��������V(XPS)����������ȸ�G��Cr(��)���Burkholderia cepacia C09G���D 4�Ǿ��w����Cr��2p܉�����ą^���XPS���V�D����M������.���Կ�����Cr2p1/2�ĽY������584.0 eV̎����Cr2p3/2�ĽY������577.4 eV̎����֪�ɂ���ֵ�cCr(��)�ĽY�������������@�f���ھ��w���摪ԓ����Cr(��)��������ǰ�����B����ֻ��Cr(��)����ˣ��Ɯy���B����Cr(��)��Burkholderia cepacia C09G�������±����������������þ��w�ȵ�߀ԭø��Cr(��)��߀ԭ��Cr(��).�����īIҲ����ƈ�������������ü���NADH����߀ԭ�����ں���������B�£����߶��Ե�Cr(��)ֱ��߀ԭ�ɵͶ���Cr(��)(Lira-Silva et al., 2011)��������Burkholderia vietnamiensis C09Vͬ�rȥ���Y���Ϻ�Cr(��)�r��ԓ���ڽ���Y���ϵ�ͬ�r��Cr(��)߀ԭ��Cr(��)(�����, 2014).
����
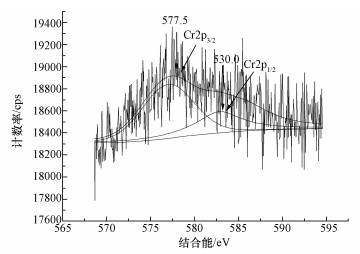
�����D 4������Burkholderia cepacia C09G��Cr2p���V�D
����3.3.2 SEM
�����ɈD 5a��֪������Һ��ֻ�п�ȸ�G���ڕr��B. Cepacia C09G�����ΑB���]���Ɠp���������������A��M�����L����.����ȸ�G��Һ�м���0.5 mmol·L-1 EDTA�r�������ΑB��Щ���ēp��(�D 5b).������Cr(��)�����:����������ܓp���������氼��ƽ��׃�øɰT(�D 5c).��D 5d��ʾ��ͬ�r����0.5 mmol·L-1 EDTA��0.5 mmol·L-1 Cr(��)���cֻ��EDTA��ȣ��������ΑBӰ������^С���c����EDTA�cCr(��)�ļ����ΑB����mȻ�ܾS���^�����ļ����ΑB��߀�������p��.�ĈD 5�п��Կ�����EDTA�cCr(��)�����Ɖļ����ĽY�����Ķ���������Ļ��ԣ�ͬ�r����EDTA��Cr(��)��EDTA�p����Cr(��)��B. Cepacia C09G�Ķ���.
����

�����D 5�����Burkholderia cepacia��SEM�D(10000×)(a.0.1 mmol·L-1 MG, b. 0.1 mmol·L-1 MG+0.5 mmol·L-1 EDTA, c. 0.1 mmol·L-1 MG+0.5 mmol·L-1 Cr(��), d.0.1 mmol·L-1 MG+0.5 mmol·L-1 EDTA+0.5 mmol·L-1 Cr(��))
����3.3.3 EDS
����ͨ�^EDS�_������B. Cepacia C09G��������MG��Cr(��)����EDTA�����ֲ�����Ԫ�أ��ĈD 6�п��Կ������D�о�����C��K��O��Na��P���@ЩԪ����Ҫ�ǁ�������������;���⣬�D 6b��6c��߀����Cr���@����������Ч��������Cr����Դ����Һ�м����K2Cr2O7.�D 6b��6c�зքe��0.48��5.40��5.96 keV̎���F�壬�@ʾ����CrԪ�أ��@���C����C09G����ȥ����ȸ�G��ͬ�rҲ��������Cr.�����ڈD 6c�c6b�Č����п��Կ�������������EDTA��Cr�ĺ������@�p�٣���0.59%���͵�0.37%���f��EDTA����ھ��ꌦCr���H��������.
����
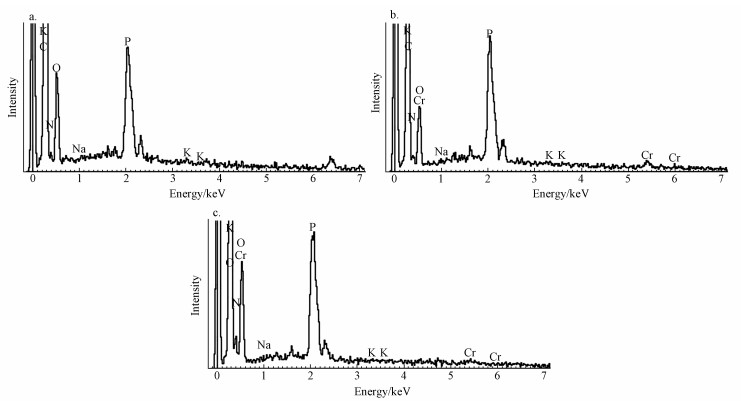
�����D 6�����Burkholderia cepacia��EDS�D(a. 0.1 mmol·L-1 MG, b. 0.1 mmol·L-1 MG+0.5 mmol·L-1Cr(��), c.0.1 mmol·L-1 MG+0.5 mmol·L-1 EDTA+0.5 mmol·L-1 Cr(��))
����3.3.4 FTIR
�����D 7�����B. Cepacia C09G������ȸ�G����ȸ�G��Cr(��)���FTIR���V�D.�ɈD 7��֪��2939~2927 cm-1̎�ķ���—CH��—CH2��—CH3�IJ����Q��ӷ壬��1655 cm-1��1546 cm-1̎���F�ɰ�����I��—NH2�c������II��—COOH�γɵ�—NH/CO����s������շ壬1408~1405 cm-1̎�քe���ȸ�G������a�﷼�h�ϵ�C=C����s��ӷ��O—H�ď�����ӷ�.�D 7b����ڈD 7a����2452 cm-1��845 cm-1̎�ķ���ʧ��1070 cm-1̎��Įa�������ڰ������—NH�D׃��C=N��ܗ�I.�@�f������C09G��ȥ���^����Ҫ��—OH��—COOH��—NH2��—NH/CO�ȹ��܈F�cCr�����(Nandi et al., 2009).
����
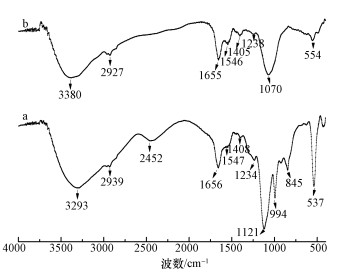
�����D 7����B. Cepacia C09G������ȸ�G(a)����ȸ�G��Cr(��) (b)���FTIR���V�D
�����ģ��YՓ(Conclusions)
����1) 0.1 mmol·L-1��ȸ�G�Ϊ����ڗl���£�24 h�����オ�����_��96.2%;Ȼ������0.5 mmol·L-1 Cr(��)����r��60 h�Ľ����ʃH��6.7%;������0.5 mmol·L-1 EDTA���τ���60 h�r��ȸ�G�Ľ�������ߵ�18.8%.�f��Cr(��)��EDTA�������ƿ�ȸ�G�Ľ��⣬����0.5 mmol·L-1 EDTA����Cr���@������Cr�Ķ���.
����2) ����0.5 mmol·L-1 EDTA�����^������Cr(��)�ĝ�Ȟ�0.7 mmol·L-1���˕r��60 h�Ŀ�ȸ�G������������35.3%��Cr�����ʞ�24.6%��������Ҳ�������.
����3) XPS�����C����Burkholderia cepacia C09G�Ɍ�Cr(��)߀ԭ��Cr(��);��SEM�D�V��֪������EDTA������Cr��B. Cepacia C09G�Ķ���;EDS�C������EDTA������B. Cepacia C09G��Cr������Ч��;FTIR�f��������C09V��ȥ���^����Ҫ��—OH��—COOH��—NH2��—NH/CO�ȹ��܈F�cCr�����.
����

������ˮ̎���O��ϵ��ʽ��
�����N�۟ᾀ��010-8022-5898
�����֙C̖�a��186-1009-4262





