����������S��ʯ���ИI�İlչ�����ӏUˮ����Ⱦ���}�՝uͻ�������Ӿ��з����ı��h�Y���������⣬�����Uˮ�^�y̎����ֱ�ӑ���������̎�����ӏUˮ�y���_�������̎��Ч����һ���������Ï������������������������オ������|�����Mһ���M������̎����K2FeO4 ����һ�N���;Gɫ��Чˮ̎�턩�����кܸߵ������λ�����F���O�������������������ӵ�ȥ��Ч���^�á����džΪ�ʹ�� K2FeO4 ̎�����ӏUˮ�����ӽ��ⲻ�صף�̎����ďUˮCODCr ���fƫ�ߡ�����Ҫԭ����K2FeO4 �����������UˮpH Ӱ��^�����ԗl���� K2FeO4 �m���к����������������Ǻܲ��������O�ֽ⣬�c���ӵķ����r�g�ܶ�;��pH �^�ߕr�������m�ã������r�g�L�������������^���������ӵĽ��ⲻ�صס�
�������о�����K2FeO4 ��NaClO ��̎��ģ�M���ӏUˮ��NaClO �ļ��룬��ʹK2FeO4 �����ԗl���µķ�������������ʹ���ھ��Џ������Ե�ͬ�r�ɱ����^�L���������ӕr�g���ɼ�����ӵĽ���̶ȣ��@����ߏUˮCODCr ȥ���ʡ�
����1 ����
����1.1 ���x����ԇ��
������Ҫ�x����723 ��Ҋ�ֹ���Ӌ���Ϻ����ܿƌW�x������˾;HH-5 ���W���������ٜy���x�����K����늷����x������˾;CJJ79-2 �p���������������h���A�ƽ̃x������˾;pHSJ-3F ����� pH Ӌ���Ϻ����ܿƌW�x������˾��
������Ҫԇ�������ӡ������ᡢ�������c���������c�����������;���F���(K2FeO4)���|���֔���86%�����W����
����1.2 ����
����ȡ50 mg/L ����ģ�M�Uˮ200 mL ��250 mL �����У���H2SO4 ��NaOH ��Һ�{��pH��Ȼ�����ڴ����������ϣ�����һ������K2FeO4( ��K2FeO4 �� NaClO)�����跴��һ�Εr�g���o��20 min��ȡ����Һ�^�V���y���VҺ�б��ӝ�Ⱥ�CODCr��Ӌ��ȥ���ʡ�
�������ӝ�Ȳ��÷ֹ��ȷ��y��;CODCr �������t��⛷����������W���������ٜy���x�y����
����2 �Y���cӑՓ
����2.1 K2FeO4Ͷ���������Ӻ�CODCrȥ���ʵ�Ӱ�
����ǰ���о���������50 mg/L �ı��ӏUˮ����pH= 8.9 �r��K2FeO4 �����ӵ�ȥ��Ч�����^�ѡ���ˣ��ڱ��ӳ�ʼ�|����Ȟ�50 mg/L��pH=8.9�������r�g��30 min �ėl���£�������K2FeO4 Ͷ���������Ӻ� CODCr ȥ���ʵ�Ӱ푡��Y���������S��K2FeO4 Ͷ���������ӣ����Ӻ�CODCr ȥ������u���ߣ���K2FeO4 Ͷ�������ӵ�1 500 mg/L �r�����Ӻ�CODCr ȥ���ʷքe�_��93.1%��54.3%;�^�m����K2FeO4 Ͷ���������Ӻ�CODCr ȥ�������Ӿ�������ˣ�K2FeO4 Ͷ������1.5 g/L �^���m�ˡ�
����2.2 pH �ͷ����r�g��K2FeO4ȥ������Ч����Ӱ�
�����ڱ��ӳ�ʼ�|����Ȟ�50 mg/L��K2FeO4 Ͷ������1.5 g/L �ėl���£�������pH �ͷ����r�g�� K2FeO4 ȥ������Ч����Ӱ푣��Y����D 1 ��ʾ��
����
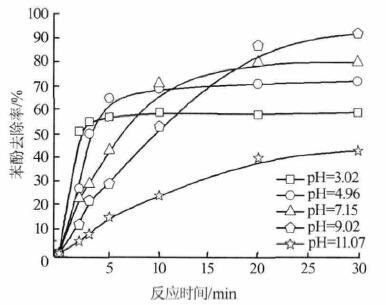
�����ɈD 1 ��֪���S�����r�g�����L������ȥ�������������_��һ���r�g����ȥ���ʵ�׃��څ��ƽ��;ͬ�r�ɈD 1 ߀�ɿ��������ӵ������ٶȺ�ȥ���ʾ����wϵpH ��Ӱ푡�pH Խ�ͣ������_��ƽ���ڵĕr�gԽ�̡���pH=3.02 �r���H����3 min ����ȥ���ʼ��_�����^��ֵ��څ��ƽ��;����pH=9.02 �r������ 20 min ����ȥ���ʲ���uڅ�ڷ���������ȥ������pH=9.02 �r���_�����^�ߣ�����pH<9.02 ��pH> 9.02 �r����ȥ���ʾ������^�͡����F�@�N�Y����ԭ���ǣ�pH Ӱ���K2FeO4 �����������ͷ����ԡ�
����K2FeO4 �����������S��pH �����Ӷ��p�����@��������늘O�λ�SpH �����Ӷ��pС���c K2FeO4 �������SpH ������pС��څ���෴���䷀���Ԅt�SpH ������������������ԗl����K2FeO4 �ķ������ܲ�O�ֽ�;�SpH �����ӣ�K2FeO4 �ķ������������ֽ��ٶ�׃����K2FeO4 �����������������c���ӵķ����r�g�L�̛Q���˱����Ƿ��ܱ��ص������ֽ⡣
����pH=3.02 �r��K2FeO4 �������ܱ��^�������s���^��������K2FeO4 ߀δ���ü��c������ȫ�����ͷֽ��ˣ��c���ӵķ����r�g�̣����±���ȥ���ʲ��ߡ�pH= 9.02 �r��K2FeO4 �������Բ�����pH �^�͵���r�¸ߣ����������^�ã��������f�c���ӵķ����r�g���L�ˣ��䌦���ӵ������ֽ������_�����^��pH=11.07 �r��K2FeO4 ���������ܱ��^������ˌ����ӵ�ȥ��Ч�����^�
����2.3 NaClO Ͷ���������Ӻ�CODCrȥ���ʵ�Ӱ�
���������о���������������^�͵�pH ����ߏUˮ��K2FeO4 �ķ����ԣ��Ķ����L���c���ӵ��������Õr�g��������Ч����߱��ӵ�ȥ���ʡ����P�@������о������^����������о�����K2FeO4 �c NaClO ��̎�����ӏUˮ���ڱ��ӳ�ʼ�|����Ȟ� 50 mg/L��K2FeO4 Ͷ������1.5 g/L��pH=5.03�������r�g��30 min �ėl���£�������NaClO Ͷ���������Ӻ�CODCr ȥ���ʵ�Ӱ푡��Y�����������Ӻ�CODCr ȥ�����SNaClO Ͷ���������Ӷ�����NaClO Ͷ������300 mg/L �r�����Ӻ�CODCr ȥ���ʷքe���_ 98.3%��69.8% ���^�m����NaClO Ͷ���������Ӻ� CODCr ȥ���ʵ�׃��څ��ƽ�����͆Ϊ�ʹ��K2FeO4 ̎�����ӏUˮ��ȣ�CODCr ȥ�����������@��NaClO Ͷ������300 mg/L �^���m�ˡ�
����2.4 pH ��K2FeO4-NaClO ��ȥ������Ч����Ӱ�
������50 mg/L �ı��ӏUˮ��Ͷ��K2FeO4 1.5 g/L �� NaClO 0.3 g/L�����첻ͬpH �ͷ����r�g�£�K2FeO4- NaClO �Ì����ӵ�ȥ��Ч�����Y����D 2 ��ʾ��
����
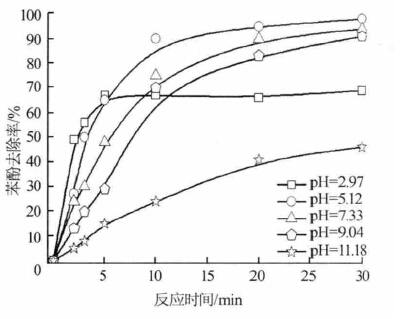
�������ȈD 1���D 2 �б���ȥ���������Ĺ��c�������ƣ�������ȥ�����_��ƽ���ڵĕr�g׃�L���f������NaClO ��K2FeO4 �ķֽ��ٶȷž��ˣ�������������ߣ��ͱ��ӵķ����r�g׃�L�ˡ�����K2FeO4- NaClO �wϵ��pH=5.12 �r����ȥ���ʱ��^�ߣ��_���� 98.5%������һ��K2FeO4 �wϵ����pH=9.02 �r����ȥ���ʱ��^�ߣ���93.1% ���@Ҳ�f����pH �^�͵���r�£�K2FeO4-NaClO �wϵ��K2FeO4 �ķ�����������
����2.5 K2FeO4��NaClO- K2FeO4�Ì����Ӻ�CODCr��ȥ��Ч������
������50 mg/L �ı��ӏUˮ�зքeͶ��K2FeO4(�UˮpH=8.93)��K2FeO4+NaClO(NaClO Ͷ������0.3 g/L���UˮpH=5.07)���ڷ����r�g��30 min �ėl���£�������K2FeO4��NaClO-K2FeO4 �����Ӻ�CODCr ��ȥ��Ч�����Y����D 3 ��ʾ��
����
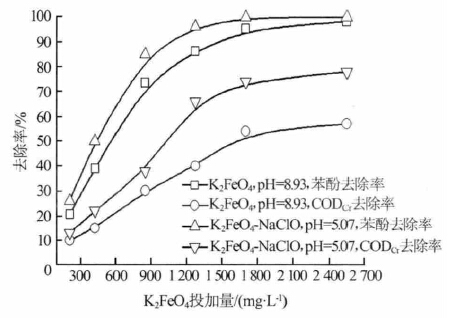
�����ɈD 3 ���Կ�����K2FeO4- NaClO �Ì����Ӻ�CODCr ��ȥ���ʺ͆Ϊ�ʹ��K2FeO4 ��ȷքe����˼s5%��25%��������ȥ���ʵ�����������CODCr ȥ���ʵ�����ʮ�����@���@�����K2FeO4 �������ӕ����ɱ��^�K�����a��CO2��H2O ��һЩ�y���������g�a�����CODCr ȥ���������^�͡�Ͷ�� NaClO ���濴������ȥ������߲������ӵ������ֽ���ȅs������ӣ��ֽ����صף����� CODCr ȥ����������@��
����2.6 NaClO-K2FeO4�ý��ⱽ�ӵĄ����W�о�
�����ڱ��ӳ�ʼ�|�����C0 ��50 mg/L���UˮpH= 5��K2FeO4 Ͷ������1.5 g/L��NaClO Ͷ������0.3 g/L �ėl���£��M����NaClO- K2FeO4 �ý��ⱽ�ӵĄ����W���Y����D 4 ��ʾ��
����
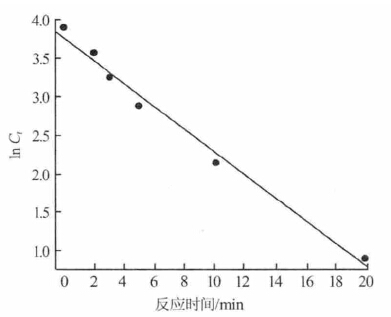
�����ɈD 4 ��֪��ln Ct �c�����r�gt �ʾ����Pϵ(Ct �鷴���r�g��t �r���ӵ�ʣ���|�����)��б�ʞ� -0.147 87�������cһ�����������W����ln (Ct /C0 )= - kt ������������ɴ˿�Ҋ��K2FeO4- NaClO ���������ⱽ�ӵ��^�̿�����һ�����������W�������������������ʳ�����0.147 87 min-1�� ���w��Ҋhttp://www.dowater.com�������P���g�ęn��
����3 �YՓ
����(1)K2FeO4 ��NaClO ̎�����ӏUˮ��Ч�����@���چΪ�ʹ��K2FeO4��CODCr ȥ�����@����ߣ������ں��m������̎����
����(2)NaClO ����Ҫ�����������K2FeO4 �����ԏUˮ�еķ����ԣ��Ķ�������K2FeO4 �c���ӵ����������r�g��
����(3)K2FeO4- NaClO �Ì����ӵĽ����^����ѭһ�����������Wģ�͡�





